Что мы знаем о первом российском препарате от коронавируса

Первый российский препарат от коронавирусный болезни «Авифавир» получил одобрение Минздрава. Разработчик препарата обещает, что уже 11 июня отправит первые партии своего лекарства в больницы. Разбираемся, откуда взялись эти жёлтые таблетки, по какому принципу работает препарат, какие клинические испытания он уже успел пройти и можно ли с определённостью сказать, что у нас появилось лекарство от COVID‑19.
Откуда оно взялось
«Авифавир» — торговое наименование российского препарата, который разработали Российский фонд прямых инвестиций (РФПИ) и группа компаний «ХимРар». Однако действующее вещество препарата было изобретено не в России.
Его международное непатентованное наименование — фавипиравир (favipiravir). Разработали его сотрудники японской компании Toyama — дочерней компании корпорации FUJIFILM Pharmaceuticals.
По своей химической структуре фавипиравир — 6‑фтор‑3‑оксо‑3,4‑дигидропиразин‑2‑карбоновой кислоты, или пиразинкарбоксамида. Во время скрининга химической библиотеки сотрудники компании Toyama обнаружили, что это вещество может обладать активностью против вируса гриппа: попав в заражённые вирусом клетки, фавипиравир превращается в активированную форму, подавляющую активность важного вирусного фермента РНК‑зависимой РНК‑.
Если «выключить» РНК‑полимеразу, вирусы гриппа утрачивают способность «печатать» в заражённых клетках свой генетический материал, РНК. В результате производство вируса, уже проникшего в клетки, останавливается. В этом состоит уникальность препарата — обычно противовирусные лекарства могут только препятствовать проникновению вирусов в клетки.
РНК‑зависимая РНК‑полимераза есть не только в вирусах гриппа, но и во всех РНК‑вирусах. Причём каталитический домен РНК‑полимеразы — так называется участок молекулы, благодаря которому фермент в принципе может работать, — во всех РНК‑вирусах устроен одинаково. А поскольку фавипиравир связывается именно с каталитическим доменом РНК‑полимеразы, у японцев были основания считать это вещество противовирусным агентом спектра действия.
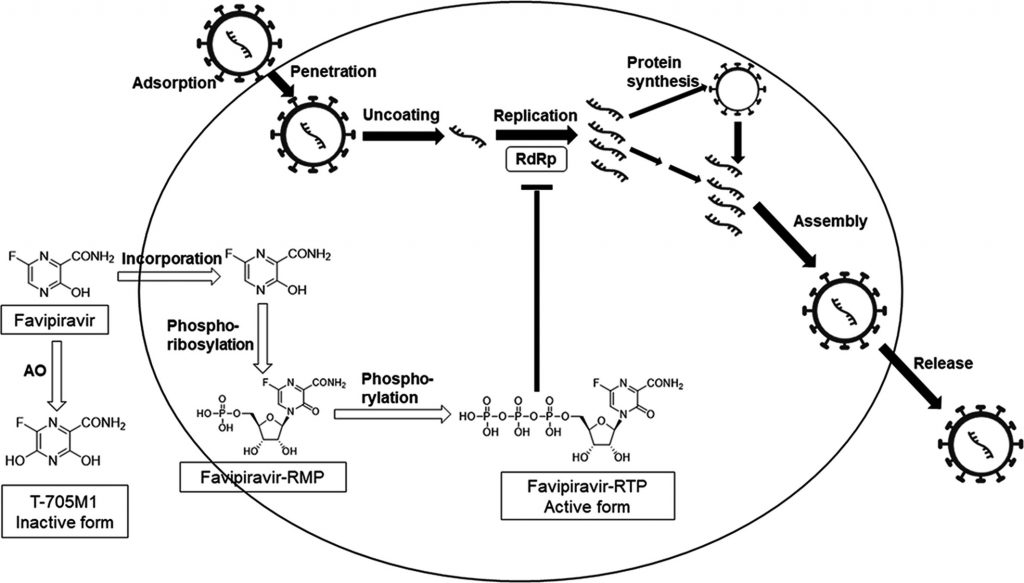
Сотрудники Toyama зарегистрировали фавипиравир под торговым названием Avigan и принялись исследовать активность многообещающего лекарства на РНК‑: от вирусов гриппа типа A и B до вируса Эбола. Результаты были неоднозначными. Например, в случае вируса Эбола выяснилось, что на макаках препарат , но во время применения на людях был не очень впечатляющим. С одной стороны, уровень летальности у 73 пациентов из Гвинеи, получавших фавипиравир, был ниже, чем у пациентов, которых пытались лечить другими способами. С другой стороны, разница была не столь велика: 42,5 процента против 57,8 процента — то есть невозможно гарантировать, что это не просто случайный артефакт подсчёта, связанный с тем, что выборка пациентов была очень небольшой. Тем не менее правительство Гвинеи этот препарат в качестве стандартного лечения против вируса Эбола.
На родине препарата, в Японии, Avigan удалось зарегистрировать только в 2014 году — и только против новых штаммов вируса гриппа. Против сезонного гриппа Avigan не использовался.

Причём препарат был одобрен не просто против «нового» гриппа, а исключительно для ситуаций, когда существующие противовирусные средства оказались неэффективными — то есть в качестве крайнего средства. За шесть лет с момента одобрения такая ситуация не возникла ни разу, так что в условиях реальной эпидемии гриппа препарат ни разу не применяли.
Обзор 29 клинических исследований (4 299 участников), шесть из которых были исследованиями второй и третьей фазы (на них уже оценивается эффективность лекарства), показали, что фавипиравир «демонстрирует благоприятный профиль безопасности»: доля серьёзных побочных эффектов 0,4 процента. Тем не менее проблемы с безопасностью препарата всё ещё остаются.
Японские исследователи, изучавшие перспективы применения препарата при тяжёлом гриппе, , что Avigan противопоказан беременным женщинам: лекарство оказывало тератогенное и эмбриотоксическое действие на животных. Другие возможные : снижение аппетита, тошнота, рвота, увеличение концентрации мочевой кислоты в крови (гиперурикемия) и повреждение печени.
Фавипиравир и COVID‑19
В марте 2020 года Чжан Синьминь, директор Национального центра развития биотехнологий, который входит в состав китайского Минздрава, , что фавипиравир «продемонстрировал хорошую клиническую эффективность против новой коронавирусной болезни (COVID‑19)». Согласно как минимум одного открытого нерандомизированного исследования, 35 китайских пациентов с коронавирусный болезнью, получавших фавипиравир (в исследовании не сказано, о каком препарате шла речь — об оригинальном Avigan или о китайском лекарстве с таким же действующим веществом), выздоровели быстрее и меньше страдали от осложнений, чем 45 пациентов, которых лечили другими лекарствами (лопинавиром и ритонавиром).
В настоящее время действенность препарата против COVID‑19 в клинических испытаниях в Японии. 9 апреля FUJIFILM о начале второго этапа клинических испытаний Avigan, который пройдёт в США, — в испытании примут участие 50 пациентов с коронавирусной болезнью. По некоторым зарубежным данным, в апреле‑мае фавипиравир тестировали ещё в 16 клинических испытаниях, но ни одного завершённого клинического испытания, которое показало бы, что фавипиравир или Avigan эффективны против коронавирусной болезни, нет.
Российский препарат
Любое лекарство состоит из действующего вещества и наполнителя (готовой лекарственной формы). Российский противовирусный препарат содержит то же действующее , что и японский препарат, — то есть 200 миллиграмм фавипиравира на таблетку. Как в разговоре с «N + 1» указал представитель РФПИ Арсений Палагин, наполнитель у российского препарата свой. В инструкции сказано, что вспомогательные вещества включают микрокристаллическую целлюлозу, кроскармеллозу натрия, коллоидный диоксид кремния, стеарат магния и повидон К‑30. Срок патентной защиты на оригинальный японский Avigan истёк в 2019 году, поэтому лекарство можно считать законно производимым дженериком.
Российские клинические испытания «Авифавира» также ещё не закончены. Завершены только первый и второй этапы многоцентрового рандомизированного исследования, подтверждает собеседник «N + 1» из РФПИ. В первом этапе приняли участие 60 человек — 20 из них вошли в контрольную группу, которая проходила лечение стандартными методами. Данные о возрастном составе и тяжести состояния испытуемых не раскрывались.
Вот что о результатах этих тестов сами разработчики:
- новых побочных эффектов в дополнение к тем, что много лет назад зафиксировали японцы, они не выявили;
- через четыре дня лечения у 65 процентов людей из экспериментальной группы тест на коронавирус дал отрицательный результат (в контрольной группе таких случаев было около 30 процентов);
- через три дня у 68 процентов людей из экспериментальной группы нормализовалась температура (у контрольной это произошло на шестой день).
Минздрав одобрил начало третьей фазы испытаний «Авифавира» 1 мая 2020 года. В этом этапе, согласно на сайте Государственного реестра лекарственных средств, должны будут суммарно принять участие 390 человек. Из тех же данных видно, что испытания фавипиравира проводят ещё две российские компании: «Технология лекарств» (входит в группу «Р‑Фарм») и «Промомед». Обе компании начали испытания в конце мая.
Хотя испытания не завершены и известны только частичные данные об эффективности, Минздрав разрешил зарегистрировать препарат досрочно — по ускоренной процедуре, принятой в рамках правительства РФ от 3 апреля 2020 года № 441. В этом постановлении говорится, что «сокращение объёма <…> экспертиз» допустимо «в условиях угрозы возникновения и ликвидации чрезвычайной ситуации».
Так что компания‑производитель уже к концу следующей недели привезти первые партии таблеток в больницы.
В к препарату написано, что она «подготовлена на основании ограниченного объёма клинических данных по применению препарата и будет дополняться по мере поступления новых данных». Тем не менее уже определены противопоказания. Как и в случае с японским Avigan, это планирование беременности, беременность и период грудного вскармливания — дженерик тоже потенциально тератогенный. Пациентам с подагрой и гиперурикемией применять лекарство нужно с осторожностью. Кроме того, список противопоказаний к российскому дженерику дополнили повышенная чувствительность к действующему веществу, возраст до 18 лет, тяжёлая печёночная и почечная недостаточность.
В аптеки лекарство поступать не будет: согласно инструкции, использовать препарат можно только в условиях стационаров.
Что в итоге
«Авифавир» — дженерик лекарственного препарата «Фавипиравира», у которого есть внятный механизм действия и который проходит клинические испытания в России и за рубежом.
Результаты промежуточных клинических испытаний показывают, что лекарство перспективное: на тех небольших выборках, что его успели проверить, лечебный эффект, судя по заявлениям разработчиков, определить удалось. Но до тех пор, пока клинические испытания не завершатся и их результаты не будут опубликованы в рецензируемых международных журналах, мы не можем быть полностью уверены, что «Авифавир» действительно помогает от коронавирусной болезни. Пресс‑служба «ХимРара», разработчика лекарства, на момент публикации этого текста на вопросы «N + 1» не ответила.
Сейчас у нас нет лекарств, которые бы целенаправленно и эффективно действовали именно против вируса SARS‑CoV‑2. Все претенденты на этот титул сейчас — вещества, известные до появление нового коронавируса, которые в клинических испытаниях (начавшихся буквально только что) стабильно показывают какой‑то положительный эффект с рядом ограничений. Их прямо сейчас — два.
Первый — это «Ремдесивир», не сходивший с первых полос в мае, — лекарство, которое ещё до эпидемии COVID‑19 предназначалось для лечения другой коронавирусной инфекции, ближневосточного респираторного синдрома (MERS). Американский регулятор одобрил клиническое применение «Ремдесивира», не дожидаясь формального окончания испытаний лекарства, — наличие стабильного эффекта в предварительных данных исследований убедило медицинских чиновников. Эту ситуацию с досрочной регистрацией , первого лекарства от ВИЧ.
При этом «Ремдесивир» никогда не претендовал на статус «серебряной пули»: испытания , что людям с тяжёлыми симптомами — которым нужна искусственная вентиляция легких, он помочь не может, а тем, у кого симптоматика легче, сокращает время болезни на четыре дня. Многие другие эффекты — например, снижение летальности болезни по сравнению с другими лекарствами — со статистической значимостью в ходе этих испытаний показать не удалось. Выборка испытаний «Ремдесивира», отчёт о которых опубликовал в конца мая журнал New England Journal of Medicine, составила 1 059 человек.
60 испытуемых — это много или мало?
Число испытуемых, необходимых для проверки эффективности препарата, рассчитывается по специальным формулам, в которых учитывается множество переменных: например, особенности показателей, которые предполагается учитывать, их разброс, уровень отклонения от показателей контрольной группы, который будет считаться клинически значимым.
Назначаются показатели, которые будут учитываться во время испытаний. Главный из них — как правило, смертность. В случае респираторных инфекций используются интегральные показатели, в которых учитывается, например, число дней с лихорадкой, время в реанимации или отделении интенсивной терапии, на ИВЛ, кашель. Все они по определённой формуле преобразуются в баллы, а затем баллы экспериментальной группы сравниваются с баллами контрольной группы.
Для каких‑то исследований достаточно будет 20 испытуемых. Для каких‑то не хватит и 2 000.
Перед началом клинических исследований могут проводиться пилотные испытания на небольшой группе. Не редкость ситуации, когда эффект, обнаруженный на группе в несколько десятков человек, впоследствии «размывается» в больших группах.
«Фавипиравир», как и «Ремдесивир», изначально не разрабатывался как средство именно против нового коронавируса. Препарат много лет назад — настолько, что патент на него уже истёк, — приспособили под лечение гриппа (строго новых вирусов, а не сезонных болезней) и испытывали против вирусов Эболы и Зика.
Да, российским исследователям, кажется, удалось поймать эффект его применения при лечении COVID‑19 — но пока на небольшой выборке в 60 человек, подробной информации о методах подбора и составе которой нет.
Так что таблетки у нас, кажется, есть. А чтобы удостовериться в том, что это действительно лекарство, придётся подождать ещё немного.














Лучшие предложения
Надо брать: лёгкий электросамокат от Segway Ninebot со скидкой 60%
Скидки до 90% на «Великой китайской распродаже» уже скоро
Долговечный каркасный бассейн от Bestway отдают со скидкой 68%
Эти 10 пар кроссовок одинаково хороши для спорта и для прогулок
Надо брать: бюджетный робот — мойщик окон от RutBot со скидкой 84%
В ожидании летней распродажи: 10 товаров из нашей корзины на AliExpress
Забираем простой в управлении водонагреватель от Midea со скидкой 33%
Умный проектор на Android от Byintek отдают по выгодной цене на AliExpress
5 способов успокоиться, если вы переживаете за экзамены ребёнка сильнее, чем он сам
Мас-рестлинг, хуреш и ещё 5 необычных национальных видов спорта России
Как стресс меняет аппетит: почему одни объедаются, а другие голодают
Как обновить квартиру: 6 простых шагов к свободному пространству и уютному дому